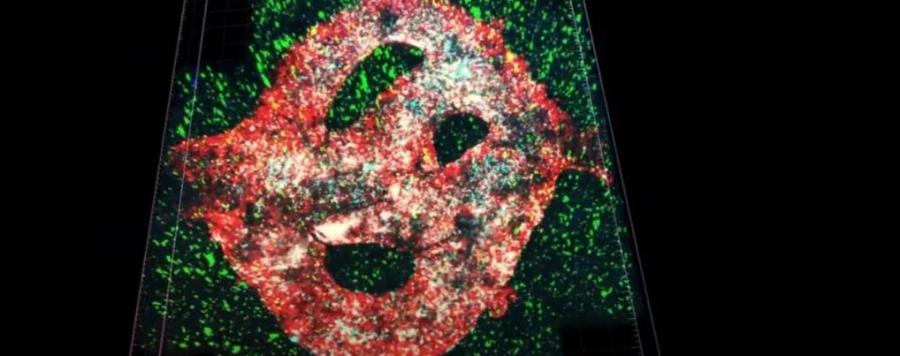
За първи път 3D принтираха смъртоносен тумор на мозъка в лаборатория
За първи път учени успешно 3D биопринтираха един от най-смъртоносните тумори на мозъка в лабораторни условия. По този начин те създадоха неговия най-пълен и отгледан в лабораторни условия модел въобще.
Учени от Университета в Тел Авив принтираха глиобластом в среда, наподобяваща мозъка – включително кръвоносните съдове, които снабдяват масата с кръв. Това е най-пълната реплика на тумор и обкръжаващата го тъкан, създавана до момента – пробив, който ще спомогне за създаването на лечения.
Глиобластомът може и да се среща рядко, но е особено ужасен. Расте бързо и агресивно по мозъка или продълговатия мозък, не може да се излекува и почти винаги е смъртоносен.
Освен това е труден за третиране. Той е особено агресивен и съответно – и терапиите трябва да са такива. Пациентите обикновено се подлагат на химио- и радиотерапия, които, уви, рядко довършват, тъй като се влошават твърде много.
Лекарите често използват тъкани на глиобластом, взети и култивирани от отстранени тумори от пациенти, за да научат повече за този рак. Това обикновено се случва в петриеви панички и може да е особено плодотворно, но има и своите ограничения, казва Ронит Сайчи-Файнаро, изследовател на рака и наноучен от Университета на Тел Авив.
В предишно проучване тя и нейният екип откриват протеин, наречен п-селектин, който се произвежда, когато раковите клетки в глиобластома се срещат с микроглиални клетки в мозъка – най-важните имунни клетки в централната нервна система.
Този протеин кара микроглията да започне да работи в полза на глиобластома, а не да се бори с него, което води до опустошителни резултати за човека.
“Ние обаче успяхме да идентифицираме протеина в тумори, отстранени по време на операция, но не и в клетки на глиобластом, отгледани в лабораторни условия в 2D петриеви панички – обяснява това. – Причината е, че ракът, подобно на всички тъкани, се държи много по-различно върху пластмасова повърхност, отколкото в човешкото тяло. Приблизително 90 процента от всички експериментални лекарства се провалят в клиничния етап, тъй като успехът, постигнат в лабораторията, не се възпроизвежда в пациенти.“
Екипът решава да преодолее това ограничение посредством био мастило на глиобластом, създадено от клетки на глиобластома, астроцити и микроглия, извлечени от пациент. С помощта на отстранимо био мастило, покрито с тип клетки, които образуват кръвоносните съдове, те успяват да снабдят своя модел с функционална кръвоносна система.
Впоследствие моделът на глиобластома е свързан (и общува) с извънклетъчна матрица посредством кръвоносните съдове – така туморът се стимулира да взаимодейства с обкръжаващата го мозъчна тъкан. По този начин учените получават шанса да изучават поведението на рака в специфична за него среда – мозъка.
„Физическите и механичните свойства на мозъка се различават от тези на други органи като кожа, гърди или кости – казва Сайчи-Файнаро. – Мозъчната тъкан се състои най-вече от мазнини, костна тъкан, която е предимно калций; всяка тъкан има свои собствени свойства, които влияят на поведението на раковите клетки и на начина, по който откликват на лекарствата. Отглеждането на всевъзможни видове рак върху идентични пластмасови повърхности не представлява оптималната симулация на клиничната среда.“
Впоследствие екипът тества своите модели чрез п-селектин. Учените вкарват инхибитор на п-селектин както в култивираните в петриеви панички глиобластоми, така и в 3D принтираните модели и животински модели. В петриевите панички не е отчетена промяна в растежа или клетъчната миграция спрямо контролните елементи в проучването, които не са били третирани с нищо.
В 3D принтираните и животинските модели обаче инхибиторът на п-селектин забавя растежа спрямо контролните нетретирани елементи.
„Този експеримент ни показа защо потенциално ефективни лекарства рядко достигат до болниците, просто защото те се провалят на тестовете в 2D модели и обратното - защо лекарства, които са постигнали феноменален успех в лабораторията, се провалят в клиничните проучвания“, допълва Сайчи-Фанаро.
Освен това генетичната секвенция и степента на растеж в 3D принтираните тумори наподобяват доста повече тези в живи пациенти. Когато се намират върху 2D петриеви панички, пробите се променят с времето и вече не съвпадат с туморите на пациентите, докато 3D принтираната глиобластома остава сходна с пробата на пациента.
Освен това всички 2D култури растат с еднаква скорост, докато 3D принтираните модели – с различна, което се наблюдава и при хора и животни.
Благодарение на новия модел учените ще могат да изучат много по-прецизно поведението на глиобластома и дори да разработят специфични за дадения пациент интервенции.
„Ако вземем проба от тъканта на пациент, заедно с нейната извънклетъчна матрица, ние можем да 3D биопринтираме от тази проба 100 миниатюрни тумора и да тестваме множество различни лекарства в различни комбинации, за да открием оптималното лечение за този специфичен тумор – казва Сайчи-Файнаро. – Но може би най-вълнуващият аспект е откриването на нови протеини и гени в раковите клетки, които да бъдат таргетирани с лекарства – подобна задача е изключително трудна, когато туморът се намира в мозъка на човешки пациент или лабораторно животно. Нашата иновация ни дава безпрецедентен достъп – без времеви ограничения – до 3D тумори, имитиращи по-добре клиничния сценарии, което от своя страна прави проучването оптимално.“
Изследването е публикувано в Science Advances.
Източник: Science Alert